Периодтық кестені қалай қолдануға болады?Білмейтін адам үшін периодтық кестені оқу ергежейлі үшін эльфтердің ежелгі рундарын қараумен бірдей. Ал периодтық кесте, айтпақшы, дұрыс қолданылса, әлем туралы көп нәрсе айта алады. Емтиханда сізге қызмет етуден басқа, ол көптеген химиялық және физикалық мәселелерді шешу үшін өте қажет. Бірақ оны қалай оқуға болады? Бақытымызға орай, бүгінде бұл өнерді кез келген адам меңгере алады. Бұл мақалада біз периодтық кестені қалай түсінуге болатынын айтамыз.
Периодтық жүйе химиялық элементтер(Менделеев кестесі) элементтердің әртүрлі қасиеттерінің атом ядросының зарядына тәуелділігін белгілейтін химиялық элементтердің классификациясы.
Кестенің жасалу тарихы
Дмитрий Иванович Менделеев қарапайым химик емес еді, егер біреу солай ойласа. Ол химик, физик, геолог, метролог, эколог, экономист, мұнайшы, аэронавт, аспап жасаушы, мұғалім болды. Ғалым өмір бойы көптеген іргелі зерттеулер жүргізе алды әртүрлі аймақтарбілім. Мысалы, арақтың идеалды күшін – 40 градусты есептеген Менделеев деген пікір кеңінен тараған. Менделеевтің арақты қалай емдегенін білмейміз, бірақ оның «Алкогольдің сумен үйлесуі туралы дискурс» тақырыбындағы диссертациясының араққа еш қатысы болмағаны және алкогольдің 70 градустан жоғары концентрациясын қарастырғаны белгілі. Ғалымның бар еңбегімен, ашқан жаңалығымен мерзімді заңхимиялық элементтер - табиғаттың іргелі заңдарының бірі, оған ең үлкен атақ әкелді.

Ғалымның периодтық жүйе туралы армандағаны туралы аңыз бар, содан кейін ол тек пайда болған идеяны аяқтауға тура келді. Бірақ, егер бәрі соншалықты қарапайым болса .. Периодтық кестені құрудың бұл нұсқасы, шамасы, аңыздан басқа ештеңе емес. Үстелдің қалай ашылғанын сұрағанда, Дмитрий Ивановичтің өзі былай деп жауап берді: « Мен бұл туралы жиырма жыл бойы ойладым, сіз ойлайсыз: мен отырдым, кенеттен ол дайын болды ».
ХІХ ғасырдың ортасында белгілі химиялық элементтерді ретке келтіру әрекеттерін (63 элемент белгілі болды) бір уақытта бірнеше ғалымдар жүргізді. Мысалы, 1862 жылы Александр Эмиль Шанкуртуа элементтерді спираль бойымен орналастырып, химиялық қасиеттердің циклдік қайталануын атап өтті. Химик және музыкант Джон Александр Ньюлендс 1866 жылы периодтық жүйенің нұсқасын ұсынды. Бір қызығы, элементтердің орналасуында ғалым мистикалық музыкалық үйлесімділікті ашуға тырысты. Басқа әрекеттердің қатарында сәттілікке ие болған Менделеев әрекеті болды.

1869 жылы кестенің бірінші схемасы жарияланды және 1869 жылдың 1 наурызы периодтық заңның ашылған күні болып саналады. Менделеев ашуының мәні атомдық массасы ұлғайған элементтердің қасиеттері біртұтас өзгермейді, периодты түрде өзгереді. Кестенің бірінші нұсқасында бар болғаны 63 элемент болды, бірақ Менделеев бірнеше элементті өз мойнына алды стандартты емес шешімдер. Сонымен, ол әлі ашылмаған элементтер үшін кестеде орын қалдыруды болжады, сонымен қатар кейбір элементтердің атомдық массасын өзгертті. Менделеев шығарған заңның түбегейлі дұрыстығы галий, скандий және германий ашылғаннан кейін көп ұзамай дәлелденді, олардың болуын ғалымдар болжаған.
Периодтық жүйенің қазіргі заманғы көрінісі
Төменде кестенің өзі берілген.
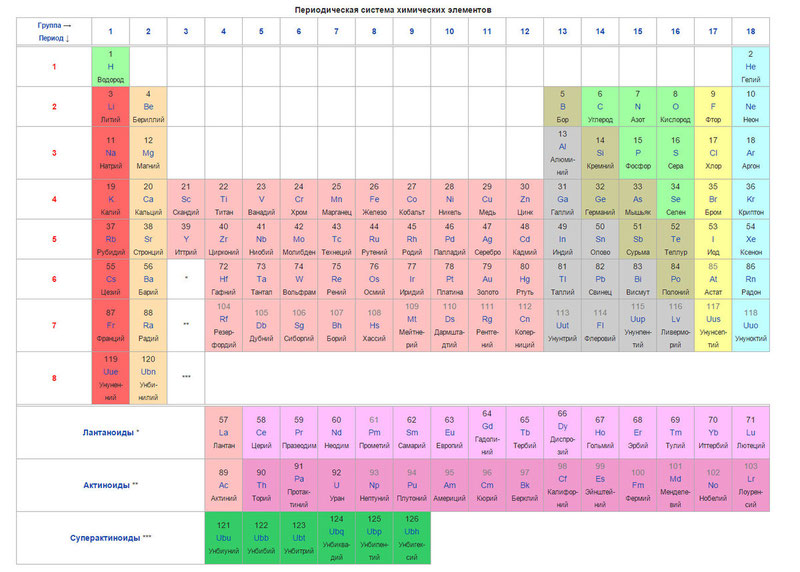
Бүгінгі таңда элементтерді ретке келтіру үшін атомдық салмақтың (атомдық массаның) орнына атомдық нөмір (ядродағы протондар саны) ұғымы қолданылады. Кестеде 120 элемент бар, олар атомдық нөмірдің (протондар саны) өсу ретімен солдан оңға қарай орналасқан.
Кестенің бағандары топтар деп аталады, ал жолдар - нүктелер. Кестеде 18 топ және 8 кезең бар.
- Элементтердің металлдық қасиеттері период бойымен солдан оңға қарай қозғалғанда төмендейді, ал кері бағытта артады.
- Период бойымен солдан оңға қарай жылжыған кезде атомдардың өлшемдері азаяды.
- Топта жоғарыдан төменге қарай жылжыған кезде тотықсыздандырғыш металдық қасиеттер артады.
- Солдан оңға қарай период бойымен тотықтырғыш және бейметалдық қасиеттер артады. I.
Кестеден элемент туралы не білеміз? Мысалы, кестедегі үшінші элемент – литийді алып, оны егжей-тегжейлі қарастырайық.

Ең алдымен элементтің символын және оның астынан оның атауын көреміз. Жоғарғы сол жақ бұрышта элементтің атомдық нөмірі кестеде орналасу ретімен берілген. Атом нөмірі, бұрын айтылғандай, санына теңядродағы протондар. Оң протондар саны әдетте атомдағы теріс электрондар санына тең (изотоптарды қоспағанда).
Атомдық масса атомдық нөмірдің астында көрсетілген (кестенің осы нұсқасында). Атомдық массаны ең жақын бүтін санға дейін дөңгелектесек, біз массалық сан деп аталатынды аламыз. Массалық сан мен атомдық санның айырмашылығы ядродағы нейтрондардың санын береді. Сонымен, гелий ядросындағы нейтрондардың саны екі, ал литийде - төрт.
Сонымен «Менделеевтің манекендерге арналған кестесі» атты курсымыз аяқталды. Қорытындылай келе, сіздерді тақырыптық бейнероликті көруге шақырамыз және Менделеевтің периодтық кестесін қалай пайдалану керектігі туралы сұрақ сізге түсінікті болды деп үміттенеміз. Жаңа пәнді үйрену жалғыз емес, тәжірибелі тәлімгердің көмегімен әрқашан тиімдірек екенін еске саламыз. Сондықтан да өз білімі мен тәжірибесін сіздермен қуана бөлісетіндерді ешқашан ұмытпау керек.
Периодтық кестенің бірі ең үлкен ашылуларбізді қоршаған әлем туралы білімді ретке келтіруге және ашуға мүмкіндік беретін адамзат жаңа химиялық элементтер. Бұл мектеп оқушыларына, сонымен қатар химияға қызығатындардың барлығына қажет. Сонымен қатар, бұл схема ғылымның басқа салаларында таптырмас.
Бұл диаграмма барлығын қамтиды адамға белгіліэлементтеріне қарай топтастырылады атомдық массасы және сериялық нөмірі. Бұл сипаттамалар элементтердің қасиеттеріне әсер етеді. Кестенің қысқа нұсқасында барлығы 8 топ бар, бір топқа енгізілген элементтердің қасиеттері өте ұқсас. Бірінші топта сутегі, литий, калий, мыс бар, олардың латынша орысша айтылуы cuprum. Сондай-ақ аргентум - күміс, цезий, алтын - аурум және франций. Екінші топта бериллий, магний, кальций, мырыш, одан кейін стронций, кадмий, барий, ал топ сынап пен радиймен аяқталады.
Үшінші топқа бор, алюминий, скандий, галлий, одан кейін иттрий, индий, лантан кіреді, ал топ таллий және актиниймен аяқталады. Төртінші топ көміртек, кремний, титаннан басталып, германий, цирконий, қалайы жалғасып, гафний, қорғасын, рутерфордиймен аяқталады. Бесінші топта азот, фосфор, ванадий, мышьяк, ниобий, сурьма сияқты элементтер төменде орналасса, одан кейін висмут танталы келіп, дубний тобын толықтырады. Алтыншы оттегіден басталады, одан кейін күкірт, хром, селен, содан кейін молибден, теллур, одан кейін вольфрам, полоний және теңізборгиум.
Жетінші топта бірінші элемент фтор, одан кейін хлор, марганец, бром, технеций, одан кейін йод, одан кейін рений, астатин және борий. Соңғы топ ең көп. Оған гелий, неон, аргон, криптон, ксенон және радон сияқты газдар кіреді. Бұл топқа сонымен қатар темір, кобальт, никель, родий, палладий, рутений, осмий, иридий, платина металдары кіреді. Одан кейін ханний мен мейтнерий келеді. Құратын бөлек орналасқан элементтер актинидтер қатары және лантанидтер қатары. Олардың қасиеттері лантан мен актинийге ұқсас.

Бұл схема элементтердің барлық түрлерін қамтиды, олар 2 үлкен топқа бөлінеді - металдар мен бейметалдарәртүрлі қасиеттерімен. Элементтің белгілі бір топқа жататынын қалай анықтауға болады, шартты сызық көмектеседі, оны бордан астатинге дейін салу керек. Мұндай сызықты тек сызуға болатынын есте ұстаған жөн толық нұсқасыкестелер. Осы сызықтан жоғары орналасқан және негізгі топшаларда орналасқан барлық элементтер бейметалдар болып саналады. Ал қайсысы төмен, негізгі топшаларда – металдар. Сондай-ақ металдар құрамындағы заттар болып табылады бүйірлік топшалар. Бұл элементтердің орналасуымен егжей-тегжейлі танысуға болатын арнайы суреттер мен фотосуреттер бар. Бұл сызықта орналасқан элементтер металдардың да, бейметалдардың да бірдей қасиеттерін көрсететінін атап өткен жөн.
Жеке тізім де қос қасиетке ие және реакциялар нәтижесінде қосылыстардың 2 түрін құра алатын амфотерлік элементтерден тұрады. Сонымен бірге олар негізгі және бірдей дәрежеде көрінеді қышқылдық қасиеттері. Белгілі бір қасиеттердің басым болуы реакция жағдайларына және амфотерлік элемент әрекеттесетін заттарға байланысты.

Айта кету керек, бұл схема жақсы сапаны дәстүрлі орындауда түсті. Бола тұра әртүрлі түстербағдарлау жеңілдігі үшін белгіленген негізгі және қосалқы топшалар. Және де элементтер қасиеттерінің ұқсастығына қарай топтастырылады.
Дегенмен, қазіргі уақытта түс схемасымен қатар Менделеевтің ақ-қара периодтық жүйесі өте кең таралған. Бұл пішін ақ-қара басып шығару үшін қолданылады. Көрінетін күрделілікке қарамастан, онымен жұмыс істеу кейбір нюанстарды ескере отырып, ыңғайлы. Сонымен, бұл жағдайда негізгі топшаны қосалқыдан айқын көрінетін реңктердегі айырмашылықтар арқылы ажыратуға болады. Сонымен қатар, түсті нұсқада электрондардың қатысуымен элементтер әртүрлі қабаттартағайындалады әртүрлі түстер.
Айта кету керек, бір түсті дизайнда схеманы шарлау өте қиын емес. Бұл үшін элементтің әрбір жеке ұяшығында көрсетілген ақпарат жеткілікті болады.

Емтихан бүгінгі таңда мектеп бітіру кезіндегі сынақтың негізгі түрі болып табылады, яғни оған дайындық міндетті түрде берілуі керек ерекше назар. Сондықтан, таңдау кезінде химиядан қорытынды емтихан, оны жеткізуге көмектесетін материалдарға назар аудару керек. Әдетте, емтихан кезінде студенттерге кейбір кестелерді, атап айтқанда, мерзімді кестені пайдалануға рұқсат етіледі жақсы сапа. Сондықтан сынақтарда тек пайда әкелу үшін оның құрылымына және элементтердің қасиеттерін, сондай-ақ олардың ретін зерттеуге алдын-ала назар аудару керек. Сізге де үйрену керек кестенің ақ-қара нұсқасын пайдаланыңызЕмтиханда қиындықтарға тап болмас үшін.

Элементтердің қасиеттерін және олардың атомдық массаға тәуелділігін сипаттайтын негізгі кестеден басқа, химияны зерттеуге көмектесетін басқа схемалар бар. Мысалы, бар заттардың ерігіштігі мен электртерістігінің кестелері. Біріншісі белгілі бір қосылыстың суда қаншалықты еритінін анықтай алады қалыпты температура. Бұл жағдайда аниондар көлденең – теріс зарядты иондар, ал катиондар, яғни оң зарядталған иондар тігінен орналасады. Білу үшін ерігіштік дәрежесісол немесе басқа қосылыстардың құрамдастарын кестеден табу керек. Ал олардың қиылысу орнында қажетті белгі болады.
Егер бұл «r» әрпі болса, онда зат қалыпты жағдайда суда толығымен ериді. «М» әрпі болған кезде – зат аздап ериді, ал «n» әрпі болғанда – ерімейді деуге болады. Егер «+» белгісі болса, қосылыс тұнба түзбейді және еріткішпен қалдықсыз әрекеттеседі. Егер «-» белгісі болса, мұндай заттың жоқтығын білдіреді. Кейде кестеде «?» белгісін де көруге болады, демек, бұл қосылыстың ерігіштік дәрежесі нақты белгісіз. Элементтердің электртерістігі 1-ден 8-ге дейін өзгеруі мүмкін, бұл параметрді анықтау үшін арнайы кесте де бар.
 Тағы бір пайдалы кесте - металл белсенділік сериясы. Онда барлық металдар электрохимиялық потенциал дәрежесін арттыру арқылы орналасады. Стресстік металдар қатары литийден басталып, алтынмен аяқталады. Солға қарай көбірек орын алады деп есептеледі осы қатарметалл, соғұрлым белсендірек болады химиялық реакциялар. Осылайша, ең белсенді металлЛитий сілтілі металл болып саналады. Сутегі элементтер тізімінің соңында да бар. Одан кейін орналасқан металдар іс жүзінде белсенді емес деп саналады. Олардың ішінде мыс, сынап, күміс, платина және алтын сияқты элементтер бар.
Тағы бір пайдалы кесте - металл белсенділік сериясы. Онда барлық металдар электрохимиялық потенциал дәрежесін арттыру арқылы орналасады. Стресстік металдар қатары литийден басталып, алтынмен аяқталады. Солға қарай көбірек орын алады деп есептеледі осы қатарметалл, соғұрлым белсендірек болады химиялық реакциялар. Осылайша, ең белсенді металлЛитий сілтілі металл болып саналады. Сутегі элементтер тізімінің соңында да бар. Одан кейін орналасқан металдар іс жүзінде белсенді емес деп саналады. Олардың ішінде мыс, сынап, күміс, платина және алтын сияқты элементтер бар.
Периодтық кесте суреттері жақсы сапада
Бұл схема химия саласындағы ең үлкен жетістіктердің бірі болып табылады. Бола тұра Бұл кестенің көптеген түрлері бар.- қысқа нұсқа, ұзын, сонымен қатар қосымша ұзын. Ең жиі кездесетіні қысқа кесте, ал схеманың ұзын нұсқасы да кең таралған. Айта кету керек, схеманың қысқа нұсқасы қазіргі уақытта IUPAC қолдану үшін ұсынылмайды.
Барлығы болды кестелердің жүзден астам түрі әзірленді, көрінісі, пішіні және айырмашылығы графикалық бейнелеу. Олар ғылымның әртүрлі салаларында қолданылады немесе мүлдем қолданылмайды. Қазіргі уақытта зерттеушілер жаңа конфигурацияларды әзірлеуді жалғастыруда. Негізгі опция ретінде тамаша сападағы қысқа немесе ұзын тізбек қолданылады.
Ол Роберт Бойл мен Антуан Лавузьенің жұмысына сүйенді. Бірінші ғалым ыдырамайтын химиялық элементтерді іздеуді жақтады. Бойлдың 15-і 1668 жылы тізімге енгізілген.
Лавузье оларға тағы 13 адамды қосты, бірақ бір ғасырдан кейін. Элементтер арасындағы байланыстың біртұтас теориясы болмағандықтан іздеу созылды. Ақыры Дмитрий Менделеев «ойынға» енді. Ол заттардың атомдық массасы мен олардың жүйедегі орны арасында байланыс бар деп шешті.
Бұл теория ғалымға ондаған элементтерді іс жүзінде ашпай-ақ, табиғатта ашуға мүмкіндік берді. Бұл ұрпақтың иығына жүктелді. Бірақ қазір бұл олар туралы емес. Мақаланы орыстың ұлы ғалымы мен оның дастарханына арнайық.
Периодтық жүйенің құрылу тарихы
Менделеев кестесі«Қасиеттердің элементтердің атомдық салмағымен байланысы» кітабынан басталды. Жұмыс 1870 жылдары жарық көрді. Осы ретте ресейлік ғалым еліміздің химия қоғамымен тілдесіп, кестенің алғашқы нұсқасын шетелдегі әріптестеріне жолдады.
Менделеевке дейін әртүрлі ғалымдар 63 элементті ашқан. Жерлесіміз олардың қасиеттерін салыстырудан бастады. Ең алдымен ол калий және хлормен жұмыс істеді. Содан кейін ол сілтілік тобындағы металдар тобын алды.
Химик дұрыс сәйкестіктер мен комбинацияларды іздеп, солитер сияқты орналастыру үшін арнайы үстел мен элемент карталарын алды. Нәтижесінде мынадай түсінік пайда болды: - компоненттердің қасиеттері олардың атомдарының массасына байланысты. Сонымен, Периодтық жүйенің элементтеріқатарға тізілді.
Химия маэстросының ашылуы осы қатарларда бос орындар қалдыру туралы шешім болды. Атомдық массалар арасындағы айырмашылықтың кезеңділігі ғалымды барлық элементтер әлі адамзатқа белгілі емес деп болжауға әкелді. Кейбір «көршілер» арасындағы салмақтың алшақтығы тым үлкен болды.

Сондықтан, Менделеевтің периодтық жүйесі«ақ» жасушалардың көптігімен шахмат тақтасы сияқты болды. Олардың шынымен де «қонағын» күткенін уақыт көрсетті. Олар, мысалы, инертті газдарға айналды. Гелий, неон, аргон, криптон, радиоакт және ксенон 20 ғасырдың 30-жылдары ғана ашылды.
Енді мифтер туралы. Солай деген пікір кең тараған химиялық кестеМенделеевоған түсінде көрінді. Бұл университет оқытушыларының интригалары, дәлірек айтсақ, олардың бірі - Александр Иностранцев. Бұл Санкт-Петербург тау-кен университетінде дәріс оқыған ресейлік геолог.
Иностранцев Менделеевті білетін және оған барған. Бірде іздеуден шаршаған Дмитрий Александрдың дәл алдында ұйықтап қалды. Ол химик оянғанша күтті де, Менделеевтің қағазды қалай алып, кестенің соңғы нұсқасын жазып жатқанын көрді.
Шындығында, Морфей оны ұстап алғанға дейін ғалымның мұны істеуге уақыты болмады. Дегенмен, Иностранцев шәкірттерінің көңілін көтергісі келді. Көргеніне сүйене отырып, геолог велосипед ойлап тапты, ол ризашылық білдірген тыңдаушыларға тез тарады.
Периодтық жүйенің ерекшеліктері
1969 жылы бірінші нұсқасынан бастап реттік периодтық жүйебірнеше рет жетілдірілді. Осылайша, 1930 жылдары асыл газдардың ашылуымен элементтердің жаңа тәуелділігін алуға болады - жүйе авторы айтқандай массаға емес, олардың реттік нөмірлеріне.
«Атомдық салмақ» ұғымы «атомдық сан» ұғымымен ауыстырылды. Атомдардың ядроларындағы протондардың санын зерттеуге мүмкіндік туды. Бұл нөмір элементтің сериялық нөмірі болып табылады.
20 ғасыр ғалымдары атомдардың электрондық құрылымын да зерттеді. Ол элементтердің кезеңділігіне де әсер етеді және кейінгі басылымдарда көрініс табады. мерзімді кестелер. ФотоТізім ондағы заттардың атомдық массасы артқан сайын реттелгенін көрсетеді.
Негізгі қағида өзгерген жоқ. Массасы солдан оңға қарай артады. Бұл ретте кесте бір емес, 7 кезеңге бөлінген. Сондықтан тізімнің атауы. Период – көлденең жол. Оның басы типтік металдар, соңы металл емес қасиеттері бар элементтер. Құлдырау біртіндеп жүреді.

Үлкен және кіші кезеңдері бар. Біріншілері кестенің басында, оның 3-і бар.Ол 2 элементтен тұратын тізімді ашады. Төменде 8 элемент бар екі баған бар. Қалған 4 кезең үлкен. 6-шы ең ұзын, оның 32 элементі бар. 4-ші және 5-ші орындарда олардың саны 18, ал 7-де - 24.
Есептеуге болады кестеде қанша элемент барМенделеев. Барлығы 112 атау бар. Аттар. 118 ұяшық бар, бірақ тізімнің 126 өрісі бар нұсқалары бар. Аты жоқ ашылмаған элементтер үшін әлі де бос ұяшықтар бар.
Барлық нүктелер бір жолға сыймайды. Үлкен периодтар 2 қатардан тұрады. Олардың құрамындағы металдардың мөлшері артық. Сондықтан түпкі жолдар толығымен оларға арналған. Жоғарғы қатарларда металдардан инертті заттарға бірте-бірте азаюы байқалады.
Периодтық жүйенің суреттерітігінен бөлінген. Бұл периодтық жүйедегі топтар, олардың саны 8. Ұқсас элементтер химиялық қасиеттері. Олар негізгі және қосалқы топшаларға бөлінеді. Соңғысы тек 4-кезеңнен басталады. Негізгі топшаларға шағын периодтардың элементтері де кіреді.
Периодтық жүйенің мәні
Периодтық жүйедегі элементтердің атаулары 112 позицияны құрайды. Оларды бір тізімде орналастырудың мәні бастапқы элементтерді жүйелеу болып табылады. Олар бұл үшін ежелгі дәуірде де күресе бастады.
Бар нәрсенің неден жасалғанын алғаш түсінгендердің бірі Аристотель болды. Ол заттардың қасиеттерін - суық пен жылуды негізге алды. Эмпидокл элементтерге байланысты 4 негізгі принципті бөліп көрсетті: су, жер, от және ауа.
Периодтық жүйедегі металдар, басқа элементтер сияқты, өте негізгі қағидалар болып табылады, бірақ заманауи нүктекөру. Орыс химигі біздің әлемнің көптеген құрамдас бөліктерін аша алды және әлі де белгісіз бастапқы элементтердің бар екенін ұсына алды.

Солай екен периодтық жүйенің айтылуы- біздің шындықтың белгілі бір моделін айту, оны құрамдас бөліктерге бөлу. Алайда оларды үйрену оңай емес. Бірнеше тиімді әдісті сипаттай отырып, тапсырманы жеңілдетуге тырысайық.
Периодтық кестені қалай үйренуге болады
бастайық заманауи әдіс. Компьютер ғалымдары Менделеевтің тізімін есте сақтауға көмектесетін бірнеше флеш-ойындар жасады. Жоба қатысушыларына әртүрлі нұсқалар бойынша элементтерді табу ұсынылады, мысалы, аты, атомдық массасы, әріптік белгіленуі.
Ойыншының қызмет саласын таңдауға құқығы бар - кестенің бір бөлігін ғана немесе оның барлығын. Біздің ерік-жігерімізде элементтердің атаулары, басқа параметрлер де жоққа шығарылады. Бұл іздеуді қиындатады. Жетілдірілгендер үшін таймер де қарастырылған, яғни жаттығулар жылдамдықпен жүзеге асырылады.
Ойын шарттары оқуды тудырады Периодтық жүйедегі элементтер сандарыжалықтырмайды, бірақ қызықты. Толқу оянады, бастағы білімді жүйелеу оңайырақ болады. Компьютерлік флеш жобаларды қабылдамайтындар көбірек ұсынады дәстүрлі жолтізімін үйрену.
Ол 8 топқа немесе 18 (1989 жылғы басылым бойынша) бөлінеді. Есте сақтауға ыңғайлы болу үшін тұтас нұсқамен жұмыс істемей, бірнеше бөлек кестелер жасаған дұрыс. Элементтердің әрқайсысына сәйкес келетін визуалды кескіндер де көмектеседі. Өзіңіздің бірлестіктеріңізге сеніңіз.
Сонымен, мидағы темірді, мысалы, тырнақпен және сынапты термометрмен байланыстыруға болады. Элементтің аты бейтаныс па? Біз суггестивті ассоциациялар әдісін қолданамыз. , мысалы, біз «таффи» және «спикер» сөздерінің басынан құрастырамыз.
Периодтық жүйенің сипаттамасыбір отырыста оқымаңыз. Сабақтар күніне 10-20 минут ұсынылады. Тек негізгі сипаттамаларды есте сақтаудан бастау ұсынылады: элементтің атауы, оның белгіленуі, атомдық массасы және сериялық нөмірі.
Мектеп оқушылары периодтық кестені жұмыс үстелінің үстіне немесе жиі қаралатын қабырғаға ілуді жөн көреді. Әдіс визуалды есте сақтау қабілеті басым адамдар үшін жақсы. Тізімдегі деректер еріксіз есте қалады.
Мұны ұстаздар да ескеріп отыр. Әдетте, олар сізді тізімді жаттауға мәжбүрлемейді, тіпті бақылау тізімінде де қарауға мүмкіндік береді. Үстелге үнемі қарау қабырғаға басып шығарудың немесе емтихандар алдында парақтарды жазудың әсерімен бірдей.
Зерттеуді бастап, Менделеев өзінің тізімін бірден есіне түсірмегенін еске түсірейік. Бірде ғалымнан үстелді қалай ашты деп сұрағанда, жауап: «Мен бұл туралы 20 жыл бойы ойладым, бірақ сіз ойлайсыз: мен отырдым, кенеттен ол дайын болды». Периодтық жүйе - қажырлы еңбек, оны аз уақытта меңгеру мүмкін емес.

Ғылым асығыстыққа шыдамайды, өйткені ол адасушылық пен тітіркендіргіш қателіктерге әкеледі. Сонымен, Менделеевпен бір уақытта кестені Лотар Мейер құрастырған. Алайда неміс бұл тізімді аздап аяқтаған жоқ және өз көзқарасын дәлелдеуде нанымды болмады. Сондықтан жұртшылық оның Германиядан келген химик әріптесі емес, орыс ғалымының еңбегін мойындады.